| Retour à la page d'accueil | Section précédente | Section suivante |
2.1 Structure primaire
2.1 La plupart des protéines ont une structure primaire linéaire.
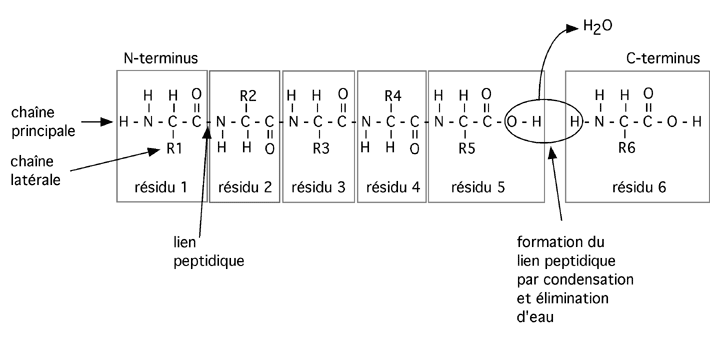
Chaque acide aminé est lié au suivant par un lien peptidique, qui se forme quand le groupement carboxylique d'un premier acide aminé réagit avec le groupement aminé d'un second, avec élimination d'eau. Quand les acides aminés sont incorporés dans une chaîne (qu'on appelle chaîne polypeptidique), on les appelle des résidus. La chaîne polypeptidique n'est pas branchée; elle forme un unique filament étiré. Par convention, on désigne le premier acide aminé de la chaîne comme étant celui dont le groupement aminé reste libre; on dit qu'il est en 5' ou encore qu'il constitue l' extremité N-terminale ou le N-terminus. On désigne comme étant le dernier résidu de la chaîne celui dont le groupement carboxylique reste libre; on le dit en 3', ou à l'extrémité C-terminale.

La figure ci-haut présente la conformation préférée du lien entre les résidus, soit en trans. Cette conformation est généralement plus stable car elle positionne les chaînes latérales loin l'une de l'autre. Qui plus est, les ribosomes synthétisent tous les liens peptidiques en trans.
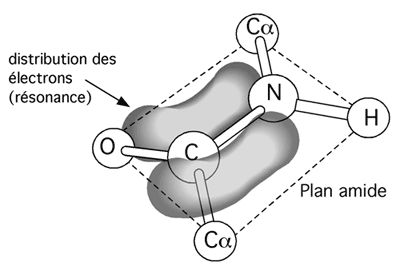
| Un effet de résonance cause le partage d'électrons entre les atomes du groupe carboxylique d'un résidu et l'azote du groupe aminé du résidu suivant. Cet effet de résonance coince le lien peptidique en une structure planaire, le plan amide. |
|
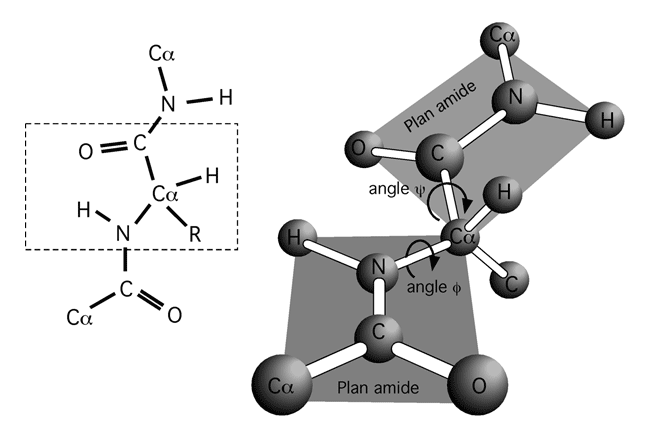
Chaque lien peptidique est donc rigide, mais de part et d'autre les liens peuvent effectuer une rotation. L'angle de rotation d'un plan amide par rapport au carbone alpha en 5' est noté angle ψ; l'angle entre le plan amide précédent et ce même carbone alpha est noté angle φ. (Voir ci-dessous). |
|
C'est la succession de ce genre de structures régulières, hélices, feuillets ou tours qu'on appelle la structure secondaire d'une protéine.
2.1.2 Il existe des protéines circulaires
En s'intéressant à l'agent actif d'un thé médicinal congolais qui facilite les contractions utérines, on découvrit dans les années 90 qu'il s'agissait d'une petite protéine de structure circulaire, assez stable pour résister à l'ébullition et à l'ingestion. Cette protéine, la kalata B1, n'était que la première d'une série de protéines circulaires que nous devions découvrir, et qui comptent maintenant plus d'une centaine de membres parmi leurs rangs (on pense qu'il pourrait même y en avoir plusieurs milliers). Leur structure leur confère une grande stabilité et plusieurs d'entre elles ont des activités insecticide ou antimicrobienne. (D'autres peptides non-protéiques circulaires existent, comme la cyclosporine dont nous avons parlé au point 1.6.2). Certaines ont en outre une structure topologique en noeud (c'est le cas de la kalata B1); on les appelle des cyclotides.
Les protéines circulaires semblent être produites à partir de grands précurseurs linéaires, mais on connait mal encore les enzymes qui permettent leur maturation et leur cyclisation. Dans le cas de la défensine RTD-1 des mammifères, deux précurseurs indépendants sont coupés et ligués ensemble à leurs deux extrémités pour former un cercle. Dans le cas du kalata B1, deux parties séparées d'un même précurseur sont d'abord coupées, puis liguées à leurs deux bouts pour former un cercle. Mais dans le cas de la bactériocine AS-48, un seul précurseur est coupé et ses deux bouts réunis pour fermer le cercle.
L'avantage d'être circulaire, pour uine protéine, est entre autres de ne pas offrir d'extrémité terminale aux exopeptidases. La stabilité en est donc accrue. Il est également plus difficile de les dénaturer de façon permanente par la chaleur ou les variations de pH.
| Retour à la page d'accueil | Section précédente | Section suivante |