BCM-514
Biochimie des protéines
2.0 Structure des protéines
2.4 Structure quaternaire
Il existe des protéines complexes formées de plusieurs chaînes polypeptidiques. L'assemblage de ces sous-unités entre elles constituent la structure quaternaire de la protéine.
2.4.1 Hémoglobine
L'hémoglobine est la molécule qui, présente dans les globules rouges, permet le transport de l'oxygène vers les tissus. Elle contribue aussi, dans une moindre mesure, à l'évacuation des ions H+ et du CO2.
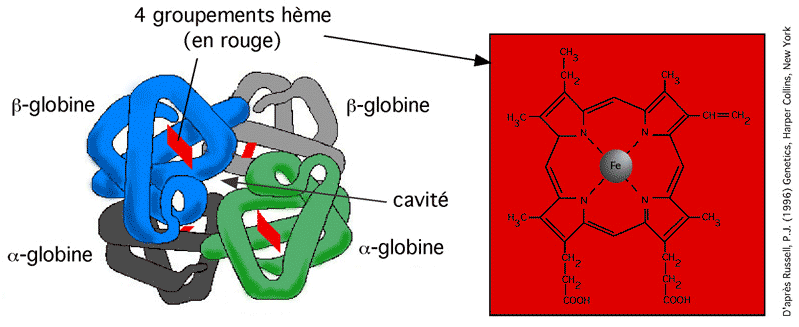
Chez l'adulte, elle est constituée de deux sous-unités d'a-globine et de deux sous-unités de b-globine. Ces sous-unités sont assemblées de telle façon qu'elles laissent une cavité au centre du tétramère. (Cette cavité ne sert pas à lier l'oxygène, mais elle a un rôle à jouer dans la régulation du rôle de l'hémoglobine, comme nous allons le voir à l'instant).
Chaque unité globine est associée à un groupe hème, qui contient un atome de fer capable, quand il est bien enligné avec ce groupe, de s'associer à l'oxygène.
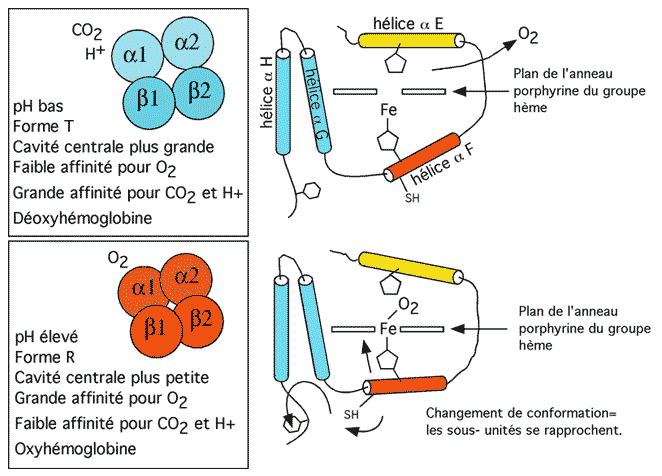
Les structures tertiaire et quaternaire de l'hémoglobine jouent un rôle primordial dans son rôle comme transporteur. La protéine existe sous deux formes, la forme T (pour tendue) qui a une faible affinité pour l'oxygène et la forme R (pour relaxée) de haute affinité. Ces deux formes existent en un équilibre rapide qui dépend du pH ambiant et de la présence d'oxygène. À pH élevé et en présence d'oxygène, la forme R est privilégiée (et l'hémoglobine cherche donc à capturer de l'oxygène); à pH bas et quand l'oxygène est rare, la forme T est privilégiée et l'hémoglobine relâche l'oxygène.
|
|
Lors d'une transition de T vers R, les sous-unités α1-β1 se rapprochent des sous-unités α2-β2, réduisant la taille de la cavité centrale entre les sous-unités. Ce changement de structure quaternaire a d'abord été remarqué lors d'expériences de cristallisation de déoxyhémoglobine: ces cristaux, mis en présence d'oxygène, se cassaient -indice que la structure des composantes du cristal avaient changé et n'était plus compatible avec le réseau cristallin initial.
En présence d'oxygène et à pH plus élevé, le mouvement de différentes hélices alpha de l'hémoglobine fait que l'atome de fer se déplace par rapport au groupement hème et vient se positionner sur le même plan (voir figure ci-bas). Cette configuration est propice à l'association du fer à une molécule de O2. Quand le pH baisse, la réaction inverse se produit: les hélices reprennent leur position typique de la forme T, la cavité centrale grandit, et l'atome de fer est déplacé par rapport au groupe hème. Il relâche alors son oxygène.
|
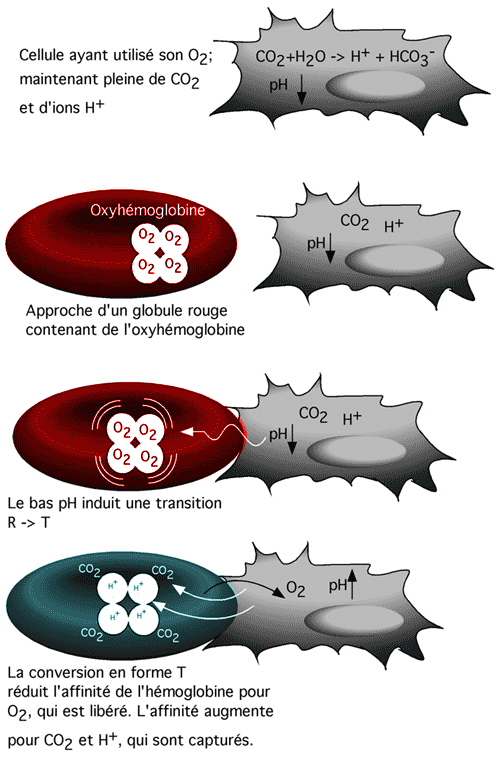
La sensibilité de l'hémoglobine au pH procède du fait que les cellules contenant beaucoup de CO2 ont un pH plus acide, parce que CO2 + H2O -> H2CO3. L'hémoglobine ayant déchargé sa charge d'oxygène peut alors contribuer à évacuer l'excédent de CO2 et d'ions H+ des cellules. Elle est responsable d'environ 20% de cette évacuation. Les ions H+ ne se lient pas au groupe hème: ils se lient à l'histidine 146 de la b-globine et à deux autres résidus dans l'a-globine de la forme T. Le CO2, lui, se lie à l'extrémité N-terminale de chacune des quatre chaînes de globine pour former la carbaminohémoglobine.
Contrairement au CO2, le monoxyde de carbone CO compétitionne directement avec O2 pour le lien libre sur l'atome de fer du groupe hème. Il a en outre une affinité 240 fois plus élevée. C'est pourquoi le CO est beaucoup plus toxique que le CO2: alors que le CO2 est libéré facilement (par simple compétition) quand le patient intoxiqué est mis en présence de O2, le CO, lui, reste fixé très longtemps sur le groupe hème, puisque l'équilibre entre le CO et O2 sur le groupe hème favorise grandement le premier.
|
La globine est une structure fort utile pour la capture de l'oxygène et on en retrouve une autre forme, la myoglobine, dans les cellules musculaires. La myoglobine n'est cependant pas un tétramère mais un monomère. En outre, elle ferait un pauvre transporteur d'oxygène parce que son affinité pour ce gaz est trop élevée (elle a tendance à le garder. Imaginez un laitier qui ne laisserait aller son lait qu'avec réticence: il ferait un bien mauvais distributeur). La myoglobine sert donc à stocker l'oxygène dans les muscles.
Chez l'hémoglobine, la capture d'oxygène par une première sous-unité entraîne une augmentation d'affinité pour les suivantes. Les sous-unités de l'hémoglobine pratiquent donc des interactions coopératives quand il s'agit de lier l'oxygène. La courbe de saturation en O2 en fonction de la pression partielle d'oxygène est sigmoïde, reflétant cette coopération.
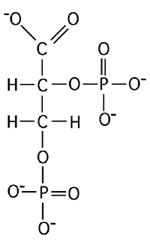
Un autre agent joue un rôle important dans la régulation de la capture d'oxygène par l'hémoglobine: il s'agit du diphosphoglycérate.
|
Le diphosphoglycérate est présent à haute concentration dans les globules rouges. Il se lie à la cavité centrale de la déoxyhémoglobine (la forme T) en interagissant avec des chaînes latérales chargées positivement dans les sous-unités de beta-globine. La transition en forme R l'expulse de la cavité. Le diphosphoglycérate réduit l'affinité de l'hémoglobine pour l'oxygène. Il est produit en plus grande quantité chez les individus fréquentant les hautes altitudes, là où la pression partielle d'O2 est plus faible, afin de faciliter la libération d'oxygène par les globules rouges.
|
2.4.2 Anémie falciforme
|
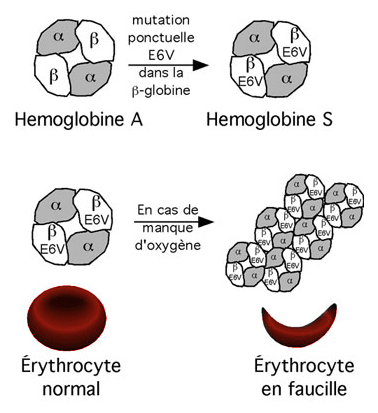
L'anémie falciforme est une maladie sanguine causée par une simple mutation: celle de l'acide glutamique en valine à la sixième position de la structure primaire de la beta-globine. Cette mutation cause une malformation de l'hémoglobine (qu'on dit "hémoglobine S"). À basse concentration d'oxygène, l'hémoglobine S précipite et forme des fibres insolubles.
Ces fibres s'accumulent dans les globules rouges qui prennent une forme en faucille, d'où le nom de la maladie. De telles hématies ne peuvent pas transporter d,oxygène et peuvent boucher les capillaires.
Ceci dit, les porteurs d'une seule allèle mutée ne souffrent que d'une forme atténuée de la maladie et gagnent un avantage: leurs globules rouges sont moins sujets à être affectés par Plasmodium, le vecteur de la malaria. pour cette raison, la mutation n'a pas été éliminée par l'évolution mais se maintient dans les régions du monde où sévit la malaria.
|
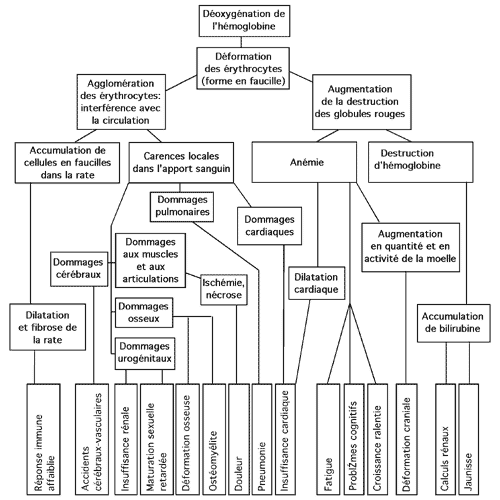
Les effets pléiotropiques d'une seule mutation dans la séquence de la beta-globine (Glu6Val) qui mène à l'anémie falciforme. (D'après Strickberger, MW, Genetics (3e éd.) Prentice-Hall, Upple Saddle River, 1985).
2.4.3 Un peu plus sur le transport de l'oxygène...
2.4.3.1 Hemerythrine
L'hemerythrine est une protéine qui sert à véhiculer l'oxygène chez les brachiopodes, les sipunculides, les priapulides et un annélide (le Magelona). Elle est incolore dans son état désoxygéné et adopte une couleur rose en absorbant l'oxygène. Contrairement à l'hémoglobine, elle ne souffre pas d'empoisonnement au monoxyde de carbone.
Elle aussi utilise le fer pour fixer l'oxygène, mais pas sous forme de groupement hème comme le fait l'hémoglobine. Deux atomes de fer y sont liés aux anneaux imidazole de cinq histidines et au groupes carboxyliques d'un acide aspartique et d'un acide glutamique. Un atome d'oxygène est également positionné entre les deux atomes de fer. L'hemerythrine est le plus souvent trouvée sous forme d'un octamère de 108 000 Da, mais il existe des formes dimériques, trimériques ou tétramériques chez certains organismes. La topologie de cette protéine est presque entièrement composée d'hélices.
2.4.3.2 Chlorocruorine
Ce sont des pigments respiratoires extracellulaires de couleur verte. On les retrouve dans le plasma de quatre familles de polychètes, parfois en même temps que de l'hémoglobine (à laquelle les chlorocruorines ressemblent énormément au point de vue moléculaire, différant seulement au niveau du groupement hème). Elles ont moins d'affinité pour l'oxygène que l'hémoglobine et la myoglobine.
2.4.3.4 Hémocyanine
Il n'y a pas que le fer qui puisse servir au transport de l'oxygène, il y a aussi le cuivre. Les hémocyanines sont des transporteurs d'oxygène utilisant ce métal. Il en existe deux types, associés à certains arthropodes (crustacés et arachnides, entre autres, et donc crabes, araignées, scorpions et limules) ou à certains mollusques (pieuvre, ormeau). La circulation chez ces organismes est très différente de ce qu'elle est chez les vertébrés: plutôt que d'être pompé à haute pression par le coeur dans des artères, le sang est distribué à basse pression dans des espaces et des sinus autour des organes internes.
L'hémocyanine désoxygénée est presque incolore et elle devient bleue lors de l'oxygénation. Elle forme différents complexes selon les organismes et peut en former atteignant des tailles de 10 millions de Daltons. Elle n'est pas aussi efficace que l'hémoglobine pour le transport de l'oxygène, ce qui cause une fatigue assez rapide suite à un effort chez certains gros mollusques (comme les pieuvres).
L'hémocyanine d'un mollusque (le keyhole limpet en anglais, un animal du genre Diodora, ressemblant à une patelle) est utilisé en immunologie à cause de son grand caractère immunogénique. Vous la rencontrerez peut-être dans un labo sous le nom de KLH (keyhole limpet hemocyanin). On couple souvent de petits antigènes à la KLH pour augmenter la réponse immunitaire.
Vous savez maintenant qui sont les vrais sang bleu dans l’évolution!!!
benoit.leblanc@usherbrooke.ca





